生物相容性检测中的热原测试与其他毒性测试区别
生物相容性检测相关服务热线: 微析检测业务区域覆盖全国,专注为高分子材料、金属、半导体、汽车、医疗器械等行业提供大型仪器测试、性能测试、成分检测等服务。 地图服务索引: 服务领域地图 检测项目地图 分析服务地图 体系认证地图 质检服务地图 服务案例地图 新闻资讯地图 地区服务地图 聚合服务地图
本文包含AI生成内容,仅作参考。如需专业数据支持,可联系在线工程师免费咨询。
生物相容性检测是医疗器械、生物材料评估安全性的核心环节,涵盖热原测试、急性毒性、细胞毒性等维度。其中热原测试因直接关联“发热反应”这一严重临床风险,与其他毒性测试在目的、机制、方法上差异显著——前者聚焦“内毒素引发的体温异常”,后者覆盖器官损伤、细胞死亡、免疫过敏等更广泛的毒性效应。理清这些区别,对精准选择检测项目、保障临床安全至关重要。
测试目的:从“发热风险”到“全面毒性排查”
热原测试的核心是解决“内毒素致热”问题——当医疗器械中的热原(主要是革兰氏阴性菌内毒素)进入血液循环,会引发高热、寒战甚至休克,这是输液反应、脊髓腔注射后高热的主要原因。因此热原测试的目的很明确:验证产品是否含有足以引发发热的热原质。
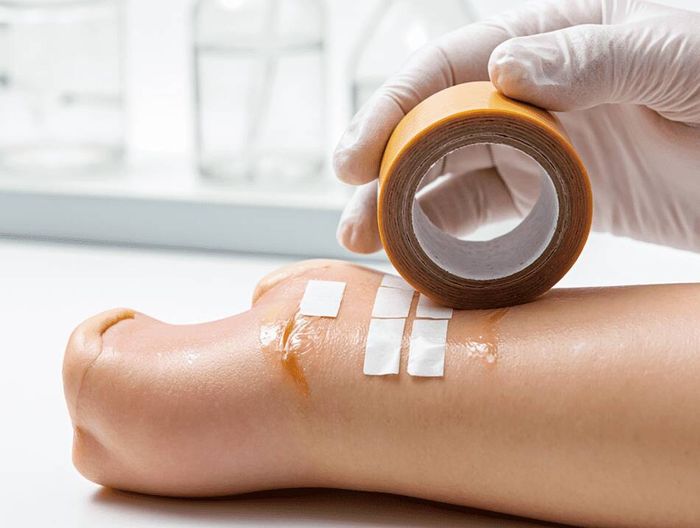
其他毒性测试的目的更广泛:急性毒性评估材料短期接触后对全身器官的损伤(如塑料增塑剂是否导致肝肾功能异常);细胞毒性看材料是否抑制细胞生长或破坏结构(如伤口敷料是否损伤表皮细胞);致敏性关注材料是否引发免疫介导的皮肤过敏(如医用胶带是否导致红斑)。
比如输液器必须做热原测试,因其内容物直接入血,热原会快速引发发热;而同一输液器的急性毒性测试是看塑料中的DEHP是否导致全身毒性,两者目标完全不同。
简言之,热原测试是“针对性解决发热问题”,其他毒性测试是“全面排查各种潜在伤害”。
反应机制:热原的“致热通路”与其他毒性的“多元损伤”
热原测试的底层机制是“内毒素激活免疫细胞释放致热因子”:内毒素(LPS)与单核-巨噬细胞表面的Toll样受体4(TLR4)结合,触发细胞释放白细胞介素-1(IL-1)、肿瘤坏死因子-α(TNF-α)等内生致热原,作用于下丘脑体温调节中枢,最终导致体温升高。
这种机制具有高度特异性——只有内毒素(或少数非内毒素热原如葡萄球菌肠毒素)能激活这一通路,其他毒性物质(如重金属、有机溶剂)不会。例如某脊髓腔注射针的热原风险来自内毒素污染,机制是LPS→TLR4→IL-1→体温升高;而其细胞毒性风险来自针尖毛刺,机制是刮伤脊髓细胞导致死亡,两者通路毫无关联。
其他毒性测试的机制更多元:急性毒性多是材料中的化学物质(如DEHP)干扰内分泌系统导致器官损伤;细胞毒性可能是材料释放的离子(如钴铬合金钴离子)抑制细胞线粒体功能;致敏性则是材料中的半抗原与皮肤蛋白结合,激活T细胞引发炎症。
比如人工心脏瓣膜的热原风险来自内毒素,细胞毒性风险来自瓣膜表面钴离子,两者机制完全不同。
检测方法:热原测试的“专属工具”与其他毒性的“通用模型”
热原测试有两种经典方法:家兔法(体内)和鲎试验(LAL,体外)。家兔法是将样品浸提液注入家兔耳静脉,观察4小时内体温变化——若体温升高超过0.5℃(或多只平均升高超过0.3℃),则判定热原阳性。这种方法模拟人体对热原的反应,因家兔体温调节机制与人类相似。
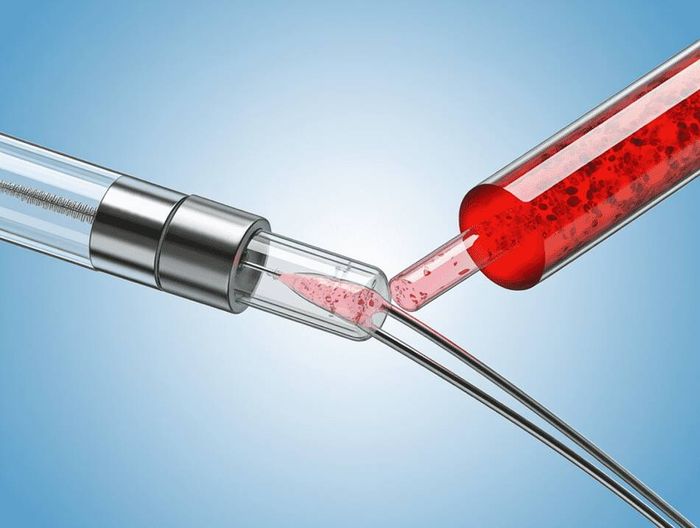
鲎试验利用鲎血中的变形细胞裂解物(LAL)与内毒素反应形成凝胶的特性,通过比浊或显色法定量内毒素浓度,适用于快速筛查内毒素污染。但它只能检测内毒素,不能检测非内毒素热原(如葡萄球菌肠毒素),因此高风险产品需两种方法结合。
其他毒性测试用更通用的模型:急性毒性用小鼠/大鼠,通过经口、皮肤接触或腹腔注射浸提液,观察14天内死亡率和器官病理改变;细胞毒性用人成纤维细胞,通过MTT法检测细胞存活率;致敏性用豚鼠,通过“致敏-激发”两步法观察皮肤反应。
比如输液器的热原测试需同时做家兔法(验证发热反应)和LAL法(定量内毒素);而其细胞毒性测试用MTT法检测细胞存活率,方法完全不同。
关注终点:热原测试的“体温/内毒素”与其他毒性的“多维度指标”
热原测试的关注终点非常明确:家兔法看“体温升高值”,LAL法看“内毒素浓度(EU/ml)”。这些终点直接关联临床风险——中国药典规定输液器内毒素限量为0.5EU/ml,若LAL测试超过此值,说明产品会引发发热,直接判定不合格。
其他毒性测试的终点更丰富:急性毒性看LD50(半数致死剂量),数值越大毒性越小;细胞毒性看细胞存活率(如≥70%为合格);致敏性看皮肤反应评分(如红斑、水肿程度);溶血看红细胞破裂百分比(如≤5%为合格)。
比如伤口敷料的细胞毒性终点是“细胞存活率≥90%”,说明不会损伤皮肤细胞;其致敏性终点是“无红斑/水肿”,说明不会过敏;而热原测试终点是“内毒素浓度<0.5EU/ml”,但因敷料不接触血液循环,热原风险极低,可能无需测试。
简言之,热原测试终点是“是否引起发热”,其他毒性测试终点是“是否导致损伤或过敏”。
适用场景:热原测试的“高风险场景”与其他毒性的“全场景覆盖”
热原测试主要适用于“直接接触血液或脑脊液的医疗器械”,因为这些场景下热原会快速进入循环,引发严重发热甚至休克。常见产品包括输液器、注射器、人工心脏瓣膜、脑脊液分流管、血液透析器等。
比如输液器的内容物直接入血,热原会在15-30分钟内引发发热;脊髓腔注射的热原直接进入脑脊液,引发的高热可达40℃以上,因此这类产品必须做热原测试。
其他毒性测试的适用场景更广泛:急性毒性适用于短期接触(≤24小时)的材料(如外科缝线、一次性手套);细胞毒性适用于表面接触的材料(如伤口敷料、隐形眼镜);致敏性适用于反复接触皮肤/黏膜的材料(如医用胶带、阴道栓剂);溶血适用于接触血液的材料(如输血器、血液滤器)。
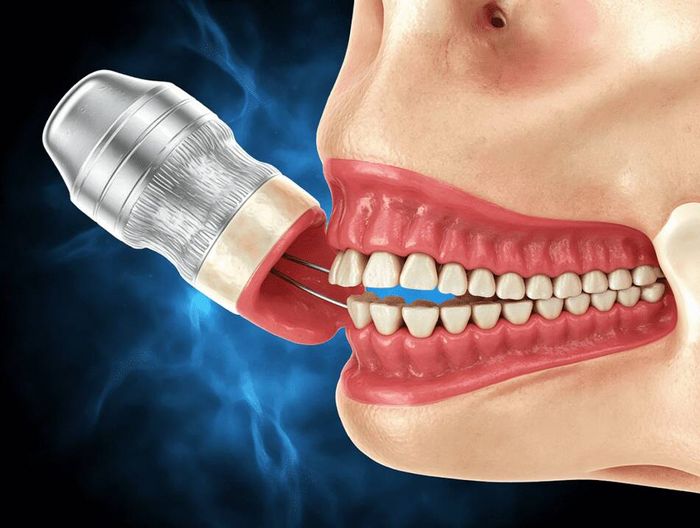
比如口腔种植体不需要做热原测试(不直接接触血液循环),但需要做细胞毒性(看种植体是否影响牙周膜细胞生长)、致敏性(看钛离子是否引起黏膜过敏)、急性毒性(看金属离子是否导致全身毒性)。
结果解读:热原测试的“一票否决”与其他毒性的“综合评估”
热原测试的结果解读非常直接:只要内毒素浓度超过阈值(如0.5EU/ml),或家兔体温升高超过标准,就判定为不合格——这种结果是“一票否决”的,无论其他测试结果多好,热原阳性的产品都不能上市。
比如某输液器的LAL测试结果为0.8EU/ml(超过0.5EU/ml限值),即使其细胞毒性、急性毒性都合格,也必须召回整改,因为它会引发输液反应。
其他毒性测试的结果需要“综合评估”:急性毒性看LD50值(如5g/kg的LD50说明毒性很低);细胞毒性看细胞存活率(如90%的存活率说明无明显毒性);致敏性看皮肤反应评分(如0分说明无过敏)。
比如某伤口敷料的细胞存活率为85%(≥70%合格),说明毒性轻微可通过;其致敏性测试为1分(轻度红斑),若临床短期使用可能也可接受,但热原测试若不合格,则直接淘汰。
干扰因素:热原测试的“特异性干扰”与其他毒性的“实验条件”
热原测试的干扰因素主要针对“内毒素检测的特异性”:LAL法会受β-葡聚糖(来自真菌)干扰,导致假阳性;家兔法会受家兔健康状况(如感冒)或环境温度(如室温过高)影响,导致结果偏差。
比如某中药注射液的LAL测试出现假阳性,后来发现是中药中的β-葡聚糖干扰了反应,需用特异性LAL试剂(排除β-葡聚糖)重新测试。
其他毒性测试的干扰因素更偏向“实验条件”:细胞毒性测试中,浸提液浓度(过高会导致细胞脱水)、培养时间(24小时vs72小时结果不同)会影响结果;致敏性测试中,豚鼠品系(Hartley豚鼠更敏感)、致敏剂浓度(过高会导致皮肤坏死)会干扰结果;急性毒性测试中,动物性别(雌性对某些化学物质更敏感)、给药途径(腹腔注射比经口更易导致毒性)会影响LD50值。
比如某细胞毒性测试结果不稳定,原因是浸提液pH值过低(pH=4)导致细胞酸中毒死亡,调整pH至7.4后结果恢复正常。
相关服务