透皮吸收测试中透皮吸收实验的方法转移(实验室间)验证要点
透皮吸收测试相关服务热线: 微析检测业务区域覆盖全国,专注为高分子材料、金属、半导体、汽车、医疗器械等行业提供大型仪器测试、性能测试、成分检测等服务。 地图服务索引: 服务领域地图 检测项目地图 分析服务地图 体系认证地图 质检服务地图 服务案例地图 新闻资讯地图 地区服务地图 聚合服务地图
本文包含AI生成内容,仅作参考。如需专业数据支持,可联系在线工程师免费咨询。
透皮吸收实验是经皮给药制剂研发与质量控制的核心技术,其结果直接关联药物的有效性与安全性评价。实验室间方法转移作为多中心研究、委托检测的关键环节,需通过系统验证确保接收实验室能稳定复现原方法的性能——若转移过程中忽略设备等效性、操作一致性等要点,可能导致数据偏差,影响研发决策或注册申报结果。本文结合透皮实验的技术特性,梳理实验室间方法转移的核心验证要点,为行业实践提供可操作的指导。
转移前预评估:识别风险与匹配基础条件
预评估是方法转移的“前置 checkpoint”,核心目标是确认接收实验室能否满足原方法的实施要求。首先需收集原实验室的方法性能基线数据:包括药物在接受液中的提取回收率(≥90%)、日内/日间精密度(RSD≤10%)、线性范围(如0.1-10μg/mL,相关系数r≥0.995),这些参数是判断方法稳定性的基础。其次评估接收实验室的硬件条件:透皮扩散仪型号、扩散池体积、检测器类型(HPLC-UV/LC-MS)需与原实验室匹配;若存在差异(如原用Franz扩散仪,接收用Logan扩散仪),需提前验证设备等效性——用标准药物(如咖啡因)测试两种设备的精密度与回收率,若RSD≤10%则视为兼容。
预评估还需覆盖“软条件”:接收实验室人员的透皮实验经验(如是否独立完成过皮肤处理、扩散仪操作)、质量体系完整性(如设备校准记录、样品管理SOP)。例如,若接收实验室无皮肤处理经验,需提前规划培训计划;若实验室无设备校准程序,需先建立校准SOP,确保扩散仪温度(32±0.5℃)、搅拌速度(600±20rpm)等参数稳定。
方法文件标准化:消除歧义的核心载体
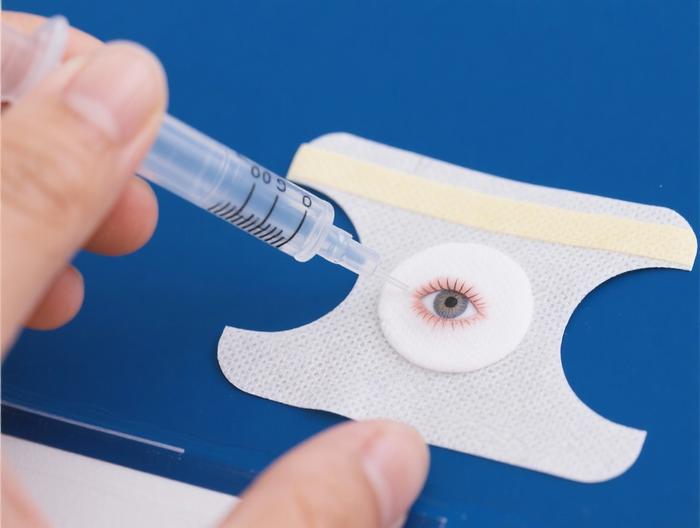
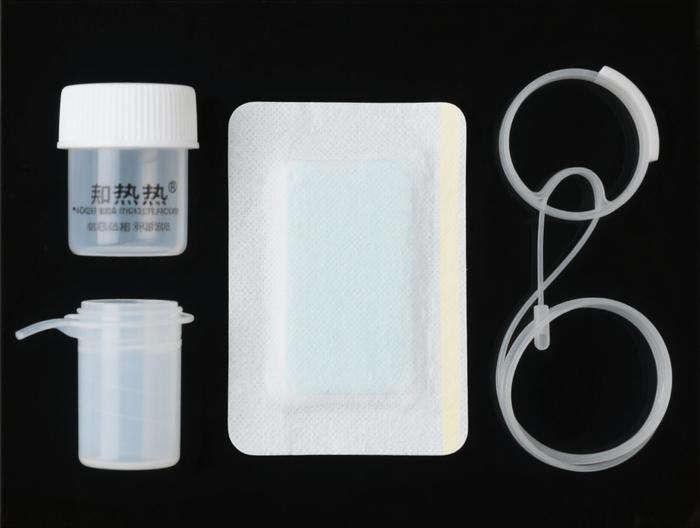
方法文件是实验室间传递技术要求的“桥梁”,需做到“精确到每一步操作”,避免模糊表述。文件应包含:实验原理(如Fick’s第一定律在被动扩散中的应用)、皮肤处理流程(猪耳皮的获取:宰杀后1小时内取耳,去除皮下脂肪至厚度≤1mm,8%硫化钠脱毛5±1分钟,生理盐水冲洗3次)、扩散池准备(75%乙醇浸泡30分钟,超纯水冲洗3次)、接受液配制(pH7.4磷酸盐缓冲液:0.68g KH2PO4+1.42g Na2HPO4·12H2O+1000mL超纯水,调pH至7.4±0.1)、操作步骤(皮肤固定:角质层朝上平铺,O型圈轻压,凡士林密封边缘)、取样规则(1/2/4/6/8/12/24小时取样,每次1mL,补加等量新鲜接受液)、数据处理(累积透皮量公式Qn=(Cn×V+ΣCi×Vi)/A,其中A为扩散面积)。
文件需避免“适量”“大约”等模糊词——例如原方法中“取适量接受液”需修改为“准确量取20mL接受液”;“适当搅拌”需明确为“搅拌速度600±20rpm”。原实验室与接收实验室的负责人需共同审核文件,确保无歧义:某案例中,接收实验室因文件中“脱毛时间约5分钟”的表述,导致脱毛不彻底(残留绒毛),药物渗透量偏低20%,修改为“脱毛时间5±1分钟”后差异消除。
关键设备:等效性验证与参数控制
透皮扩散仪是实验的核心设备,其性能差异会直接影响结果。若接收实验室与原实验室的扩散仪型号不同(如Varian VK7010 vs Logan 912-4),需通过“设备等效性验证”确认兼容性:用同一批猪皮、同一接受液测试标准药物(如咖啡因),计算累积透皮量(Q24h)的RSD。若RSD≤10%,说明两种设备性能等效;若RSD>10%,需调整参数(如将Logan扩散仪的搅拌速度从500rpm提高至600rpm),直至等效性满足要求。
除扩散仪外,检测器的一致性也需关注。例如原实验室用HPLC-UV检测,接收实验室用HPLC-FLD,需验证检测器的灵敏度与线性:用标准溶液测试两种检测器的最低定量限(LOQ),若FLD的LOQ比UV低一个数量级,需调整样品浓度,确保检测结果在 linear range 内。
实验材料:来源与处理的一致性要求
皮肤是透皮实验中最关键的材料,其屏障功能的差异会导致药物渗透速率的显著变化。皮肤来源需一致:若原实验室用猪耳皮,接收实验室不能随意改用大鼠背部皮肤(猪耳皮角质层厚30μm,大鼠皮肤厚15μm,渗透速率差异可达2倍)。若必须更换皮肤来源,需进行“皮肤 equivalency test”:用原方法的药物测试两种皮肤的渗透速率,若差异≤15%,可替代使用。
皮肤的处理流程需严格一致:从动物处死后1小时内取皮,去除皮下脂肪至厚度≤1mm(眼科剪平行修剪),8%硫化钠脱毛5±1分钟,生理盐水冲洗3次(每次1分钟),然后浸泡在生理盐水中30分钟恢复屏障功能。皮肤的保存条件也需一致:-20℃冷冻保存,使用前37℃生理盐水解冻30分钟,避免反复冻融(会破坏皮肤结构)。
接受液与其他材料的一致性同样重要。接受液需按原配方精确配制:pH7.4磷酸盐缓冲液需用pH计校准至7.4±0.1,避免pH偏差导致药物解离度变化(如弱酸性药物在pH6.8接受液中渗透量会降低25%)。扩散池的膜需用同一材质(如纤维素膜,孔径0.45μm),避免不同膜的通透性差异影响结果。
预实验:验证方法可行性的关键步骤
接收实验室需通过预实验验证能否复现原方法的结果。预实验设计:取3批样品(高/中/低剂量),每批6个平行样(降低透皮实验的变异性),严格遵循原方法操作。核心对比指标包括:累积透皮量(Q24h)、渗透速率(J,稳态透皮速率)、滞后时间(tlag,药物开始渗透的时间)。
例如原实验室某药物的Q24h历史数据为120±10μg/cm²,接收实验室预实验的Q24h为115±8μg/cm²(差异4.2%≤15%)、J为5.0±0.4μg/(cm²·h)(RSD7.8%≤10%)、tlag为1.5±0.2小时(差异6.2%≤20%),说明方法可行。若预实验数据不符合要求,需逐一排查:某接收实验室Q24h为90±5μg/cm²(低25%),检查发现皮肤固定过松,扩散池边缘漏液,接受液体积减少——用凡士林密封边缘后,Q24h升至118±7μg/cm²,符合要求。
预实验中需严格检查皮肤完整性:每批实验后用0.1%亚甲蓝溶液涂抹皮肤,若出现蓝色斑点,说明皮肤破损,该样品数据无效。某案例中,接收实验室因皮肤破损(未检查),导致某样品Q24h为200μg/cm²(是平均值的2倍),剔除破损样品后数据恢复正常。
人员能力:操作一致性的保障
透皮实验的操作细节多,人员经验直接影响结果——例如脱毛时用力过大可能损伤角质层(透皮量升高)、取样时未混匀接受液(浓度偏低)、数据处理时公式引用错误(Qn计算偏差)。因此接收实验室人员需接受原实验室的系统培训。
培训内容包括:皮肤处理技巧(用纱布轻擦脱毛后的皮肤,避免损伤)、扩散池固定(皮肤平铺无褶皱,O型圈轻压)、取样操作(取样前搅拌10秒,从中心取1mL,避免死体积)、数据处理(Excel公式验证:用标准数据测试公式正确性)。培训后需考核:让人员独立完成一次实验,原实验室资深人员评估操作符合率(如时间点取样准确性、参数记录完整性)。某人员因脱毛时用力过大(皮肤红肿)考核不合格,重新培训后学会“纱布蘸取硫化钠轻涂”,考核通过。
异常数据:规范调查与纠正
透皮实验易出现异常数据(如某样品透皮量是平均值的2倍),需建立规范的调查流程:第一步检查皮肤完整性(亚甲蓝染色,蓝色斑点=破损);第二步检查设备参数(温度是否32±0.5℃、搅拌速度是否稳定);第三步检查样品(是否按配方配制、是否过期);第四步检查仪器(HPLC基线是否平稳、柱子是否污染)。
调查需详细记录:某样品编号S001,8小时透皮量200μg/cm²(平均值100μg/cm²),检查发现皮肤有2mm破损——纠正措施:更换皮肤重新实验,新数据105μg/cm²;预防措施:每次实验前用电阻抗仪测试皮肤电阻(正常>10kΩ,破损<5kΩ),避免使用破损皮肤。
相关服务